今天的主角依旧是大家熟知的环状RNA,相信大家通过云序课堂的学习对今天的主角都是熟读在心。那小伙伴们还记得我们都上过那些关于主角的课程呢?这里不妨跟随小编回顾一下主角的奇迹之旅:
Nature Communications:环状RNA 参与干细胞分化
circRNA再发IF=18.88高分文章--你想知道的circRNA机制研究,都在这儿......
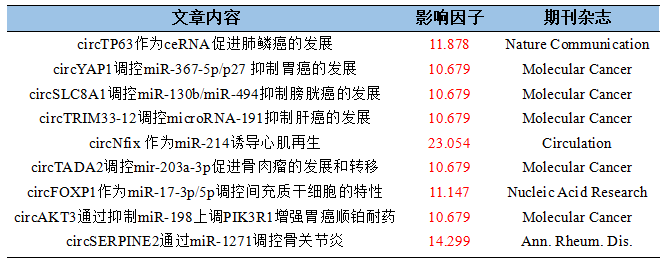

影响因子:11.878
实验方法:高通量筛选,RIP,RNA pull down等。
实验样本:上海胸科医院肺鳞癌肿瘤组织样本(T)和癌旁组织(N), 40 vs 40
(高通量筛选,5 vs 5;q-PCR验证,35 vs 35)
1.筛选肺鳞癌关键环状RNA分子-circTP63
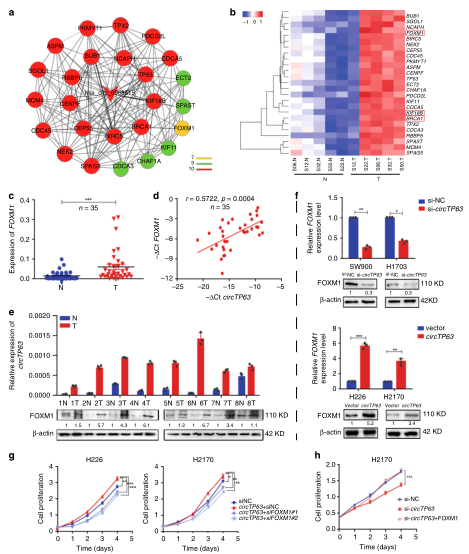
作者通过对5对肺鳞癌组织和癌旁组织高通量筛选(云序提供此服务)分析识别出7081个异常表达的环状RNA和2832个差异表达mRNA,经过circRNA和mRNA共表达网路图以及KEGG信号通路分析,预测6个circRNA和79mRNA与细胞周期调节相关。为了进一步确定候选基因排除假阳性结果,作者利用q-PCR和RNase R耐受性实验,发现hsa-circ-0068515(circTP63)在肺鳞癌组织中显著性上调且对RNase R具有耐受性。通过对另外35对肺鳞癌组织和癌旁组织q-PCR实验,证实了circTP63在肺鳞癌组织中明显上调,而且circTP63的表达与TB63表达呈正相关。显然circTP63在LUSC中上调,且其调节与临床晚期相关。
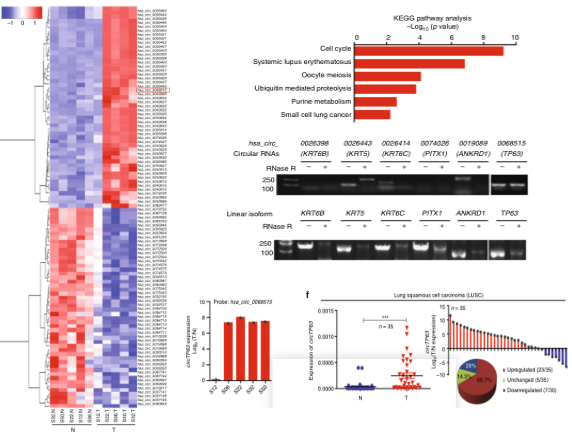
图1. 筛选circTB63
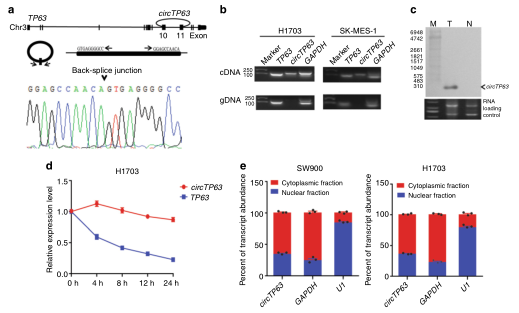
circTP63在肺鳞癌细胞中的特征。a. circTP63来源于基因组上的位置以及剪切位点;b. cDNA和基因组DNA (gDNA)中circTP63及其线性TP63的PCR分析;c. Northern blot分析LUSC肿瘤组织和相应的邻近非肿瘤组织样本中circTP63的大小和丰度;d. qRT-PCR检测放线菌素D处理H1703细胞在指定时间点的circTP63和TP63的丰度;e. circTP63在细胞中的定位。
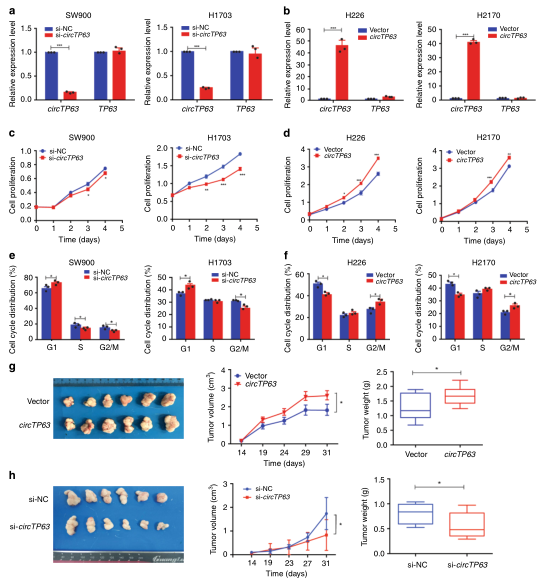
(1)如何寻找circTP63的靶基因?
本文中作者利用circTP63和mRNAs共表达网络图,发现了25个潜在的mRNA参与肺鳞癌的发展,其circTP63中FOXM1,KIFI8B和BRCA1是预测前三共表达的mRNA,而且在LUSC中FOXM1是明显上调8倍多。通过qRT-PCR和Western blots实验进一步验证了circTP63沉默明显降低FOXM1 mRNA和蛋白的表达水平,同时FOXM1沉默和过表达明显影响细胞的生长和细胞的周期发展,因此作者说明circTP63可能通过靶向FOXM1调控LUSC细胞的增殖。
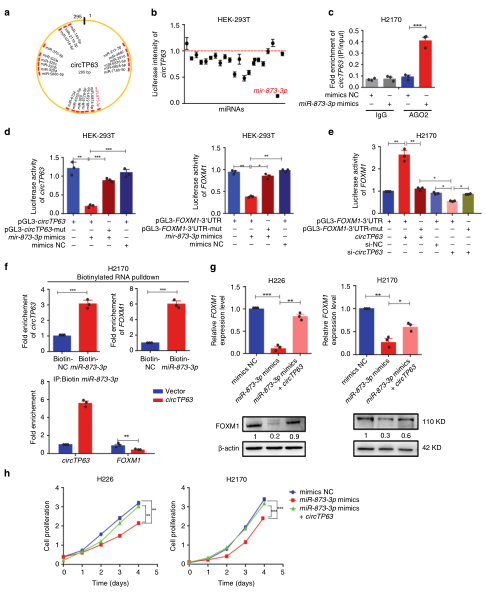
作者根据报道了解到circTP63常常以miRNA海绵机制调节下游靶基因,猜想在肺鳞癌中同样发挥竞争性内源基因的作用。通过生信分析构建circTP63-miRNAs-FOXM1网络图,发现circTP63和FOXM1的共同结合位点,荧光酶实验分析表明miR-873-3p显著性降低 circTP63的荧光活性表达,并且AGO2 RIP(云序提供此服务)也显示下拉的分子中富含大量的circTP63。利用RNA pull down(云序提供此服务)实验也发现circTP63和FOXM1复合物富集大量的miR-873-3p,过表达miR-873-3p同系物显著降低circTP63和FOXM1荧光素酶活性,而miR-873-3p抑制剂却能增加FOXM1 mRNA和蛋白的表达。原来circTP63是通过经典的海绵机制吸附miR-873-3p上调FOXM1的表达,促进肺鳞癌的生长发展,终于揭开了环状RNA在肺鳞癌中的分子机制,使得circTP63成为一个潜在治疗肺鳞癌的靶点。
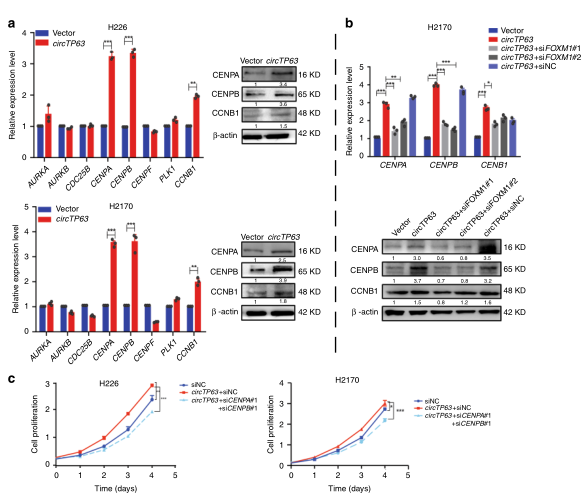
根据上述研究报道,作者继续深入研究发现circTP63能够改变肺鳞癌细胞的周期发展,那么circTP63是如何调控细胞周期的呢?FOXM1已经被证实是一个重要的细胞周期调节器,它控制细胞从G1期到S期以及到M期转变的过程。作者选择了FOXM1可能的8个下游靶基因,通过q-PCR检测到circTP63过表达时CENPA、CENPB和CCNB1显著性上调,回补实验和表型实验都证实了CENPA和CCNPB能够影响细胞的增殖。
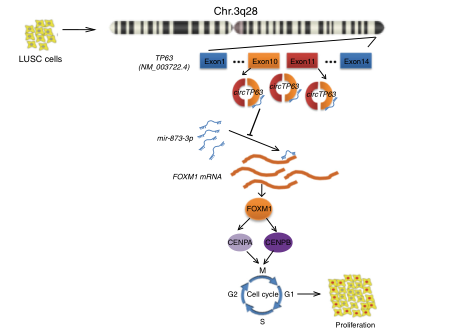
本文作者清楚地阐述环状RNA在肺鳞癌中的分子机制,即circTP63竞争性结合miR-873-3p,消除miR-873-3p对FOXM1的抑制作用,进而促进细胞增殖。国内高死亡率的肺癌终于从环状RNA分子层面解开其面纱,使得针对肺鳞癌的治疗和靶向药物分子有了新的方向,提供了一个深入了解LUSC的进展途径以及潜在的治疗方法,环状RNA分子可以成为肺鳞癌治疗潜在的药物靶向分子。
通过文章发表来看,环状RNA分子依旧是表观转录组学研究中耀眼的明星,其最经典的分子机制就是海绵作用,往往能够发表高分文章究其原因是microRNA前期研究奠定了扎实的科研基础。毫无疑问,环状RNA主角光环一直都在科学前沿,并且云序生物提供环状RNA系统性解决方案(环状RNA机制研究,“一站”到底),此时不研究环状RNA,更待何时!
https://www.nature.com/articles/s41467-019-11162-4.pdf
云序拥有系统性环状RNA服务平台,从高通量筛选到机制解析,帮助客户全面解析环状RNA。不仅如此,云序生物自行建立并维护的环状RNA数据库circDB,凭借物种覆盖广、数据量大、疾病背景多的特点为客户提供优质的服务。因此云序积累了超过10000例环状RNA测序的经验,样本覆盖20多个物种以及50多种疾病,在环状RNA文章发表方面为客户打造了多项世界第一。回首过去,从表观遗传学到表观转录组学,从基因组到蛋白质组,从细胞内到外泌体,云序生物依托于高通量测序技术为越来越多的临床与基础生物研究者提供了高质量的科研服务。相信云序生物“一站到底”服务会给更多的客户带来更优质的体验,帮助客户发表优质的文章。

相关咨询
杨宝峰院士团队RNA修饰又一成果 | 云序ac4C acRIP-seq助力揭示心脏I/R损伤的作用机制 (2024-12-03T00:00 浏览数:17977)
杨宝峰院士团队最新成果 | 云序助力揭示RNA修饰m7G调控心肌肥厚的机制研究 (2024-11-13T00:00 浏览数:18947)
Nature子刊| 重磅综述!一文总结「m6A修饰非编码RNAs」在各类肿瘤中的调控机制及作用 (暂无发布时间 浏览数:13980)
研究速览-eccDNA 2023年最新进展大放送! (暂无发布时间 浏览数:17015)
云序生物MeRIP-qPCR技术干货 (暂无发布时间 浏览数:16648)
技术干货| “eccDNA碱基序列的获取及引物设计”方法教程 (暂无发布时间 浏览数:15202)
云序客户m6A高分文章|揭示组蛋白乙酰化与m6A修饰在眼部黑色素瘤发生中的共同作用机制 (暂无发布时间 浏览数:8275)
Nat Biotechnol IF=47 | BID-seq:一种基于单碱基分辨率的假尿嘧啶(Ψ)修饰定量测序检测方法 (暂无发布时间 浏览数:8307)
北大伊成器团队Nature Reviews重磅发文:非m6A热门修饰调控与功能一文速览! (暂无发布时间 浏览数:12866)
用户文章m6A专题|IF=9.8|m6A去甲基化酶ALKBH5缺乏会加重钴致神经退行性损伤 (暂无发布时间 浏览数:8188)
